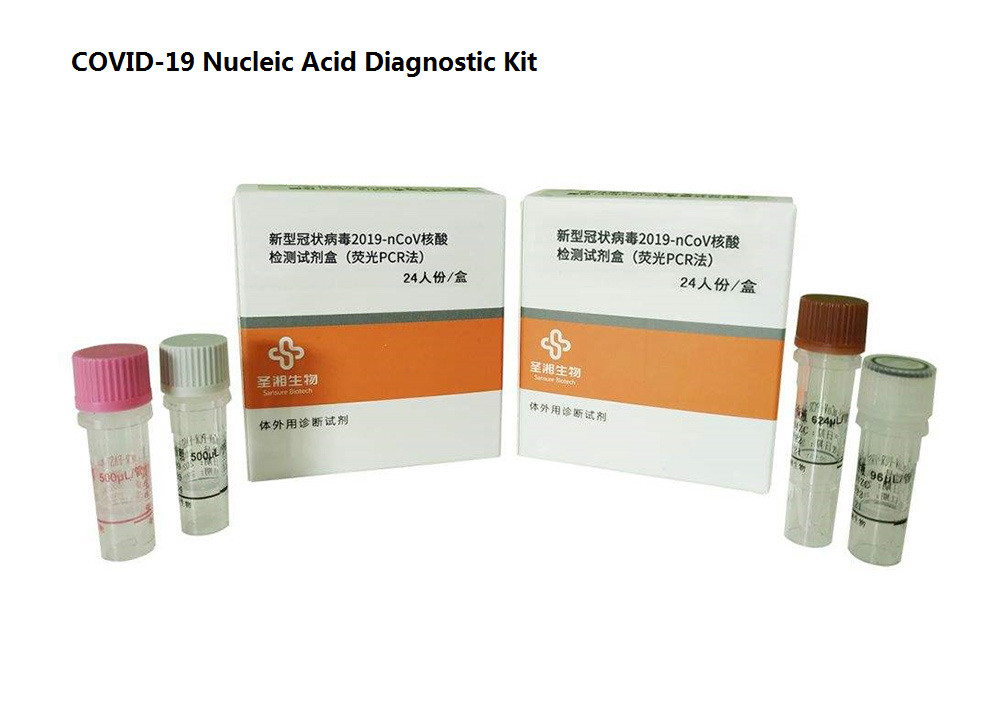
Neue Coronavirus (2019-nCoV) Nukleinsäure-Diagnoseausrüstung
(PCR-Fluoreszenz-Untersuchung)
Beabsichtigter Gebrauch
Neue Coronavirus (2019-nCoV) Nukleinsäure-Diagnoseausrüstung (PCR-Fluoreszenz-Untersuchung) wird für qualitative Entdeckung der ORF1ab- und n-Gene des neuen coronavirus (2019-nCoV) im Nasenrachenraumputzlappen, oropharyngeal Putzlappen, alveolare Waschungsflüssigkeit, Sputum, Serum, Vollblut und Rückstände von vermuteten Pneumoniefällen mit neuer coronavirus Infektion, Patienten mit vermuteten Gruppen neuer coronavirus Infektion und andere Patienten, die Diagnose oder Differentialdiagnose neuer coronavirus Infektion fordern benutzt.
Für nur in-vitrodiagnosegebrauch. Für nur Berufsgebrauch.

Zusammenfassung
Die Definitionen von „vermuteten Fällen“ und „vermuteten, dass Gruppen von Patienten“ definiert werden, indem man die „Pneumonie-Diagnose und das Behandlungs-Programm für neue Coronavirus-Infektion“ und „auf das Pneumonie-Fall-Überwachungsprogramm für neue Coronavirus-Infektion sich bezieht“, die durch China CDC herausgegeben wird (das currentversion).
Neues Coronavirus (2019-nCoV) Nukleinsäure-Diagnoseausrüstung (PCR-Fluoreszenz-Untersuchung) nur für die zusätzliche Diagnose von in Verbindung stehenden Argumenten und die Notreserve für in-vitrodiagnose während des Pneumonieausbruchs neuer Infektion Coronavirus (2019-nCoV) seit December2019 benutzt wird, diese Ausrüstung, sollte nicht als Routinein-vitrodiagnose in der klinischen Praxis verwendet werden. Folgen Sie bitte den relevanten Anforderungen der „Pneumonie-Diagnose und des Behandlungs-Programms für neue Coronavirus-Infektion“, „Pneumonie-Verhinderung und Steuerprogramm für neue Coronavirus-Infektion“ und anderen gebräuchlichen Dokumenten.
Die neuen Nukleinfeuerproben Coronavirus sollten mit „technischen Richtlinien für Laborversuche von neuem Coronavirus in China CDC“ übereinstimmen und gute Biosicherheit halten.
Komponenten der Diagnoseausrüstung
Diese Ausrüstung ist ein Verstärkungsreaktionsreagens und enthält die folgenden Komponenten:

Anmerkung:
1. Mischen Sie nicht oder tauschen Sie Komponenten von den verschiedenen Ausrüstungslosen aus.
2. Alle biologischen Proben in der Diagnoseausrüstung sind inaktiviert worden.
3. Materialien erfordert aber nicht bereitgestellt: DNAse-freie und RNase-freie Zentrifugenrohre 1.5ml, Reaktionsrohre PCR-0.2ml, Pipettenspitzen (10μL, Spitzen 200μL and1000μL mit Filtern werden bevorzugt), Tischplattenzentrifuge, verschiedene Modelle des Tischplattenturbulenzmischers von den Pipettengewehren.
4. Selbst-vorbereitetes Reagens: Beispielfreigabe-Reagens (Referenznummer: S1014E) oder Beispielfreigabe-Reagens (Referenznummer: S1015E) oder der Nukleinsäure-(DNA/RNA) Extraktion oder Reinigungs-Ausrüstung (magnetische Perlenmethode) (Referenznummer: S1002E) hergestellt durch Sansure Biotech Inc.- oder QIAamp-Viren-RNS Mini Kit (50) hergestellt durch QIAGEN. Beispielspeicher-Reagens, wie Beispielspeicher-Reagens (Referenznummer: X1002E) hergestellt durch Sansure Biotech Inc.
Qualitätskontrolle

Das Testergebnis wird als gültiges behandelt, wenn alle Bedingungen im oben erwähnten für den gleichen Test getroffen werden. Andernfalls wird das Testergebnis behandelt, wie ungültig und muss erneut getestet werden.
Bezugsbereich
Durch die Forschung auf Bezugswerten, wird der Ct-Bezugswert des Zielgens bestimmt, um 40 zu sein, der Ct-Bezugswert der internen Steuerung wird bestimmt, 40 zu sein.
Erklärung des Entdeckungs-Ergebnisses

Es gibt keine typische S-Formverstärkungskurve, die an FAM-, ROX- und HEXEN-Kanal ermittelt wird (kein Ct) oder an Ct > 40. Es wird angezeigt, dass die Konzentration des Exemplars zu niedrig ist, oder es gibt Störungssubstanzen, die die Reaktion hemmen. Das Testergebnis ist ungültig. Eine Untersuchung sollte durchgeführt werden, um die Gründe herauszufinden und auszuschließen, sammelt bitte Exemplar wieder und testet die Exemplare erneut.
Lagerung und Stabilität
1. Die Diagnoseausrüstung sollte in einem Siegelbeutel at-20±5°C gespeichert werden und vor Licht geschützt werden. Die Ausrüstung ist provisorisch für 6 Monate gültig.
2. Beziehen Sie bitte sich das Herstelldatum und auf Verfallsdatum an der Umverpackung.
3. Die Reagenzien halten gültig und stabil innerhalb des Verfallsdatums, wenn sie nicht benutzt werden. Solange der Behälter des Reagens geöffnet ist, sollten Frost/die Tauwetterzyklen drei nicht übersteigen.
 Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!  Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten!
Ihre Nachricht muss zwischen 20 und 3.000 Zeichen enthalten! Bitte überprüfen Sie Ihre E-Mail!
Bitte überprüfen Sie Ihre E-Mail!